NOTÍCIAS
CORONAVÍRUS
#EnergiaNews
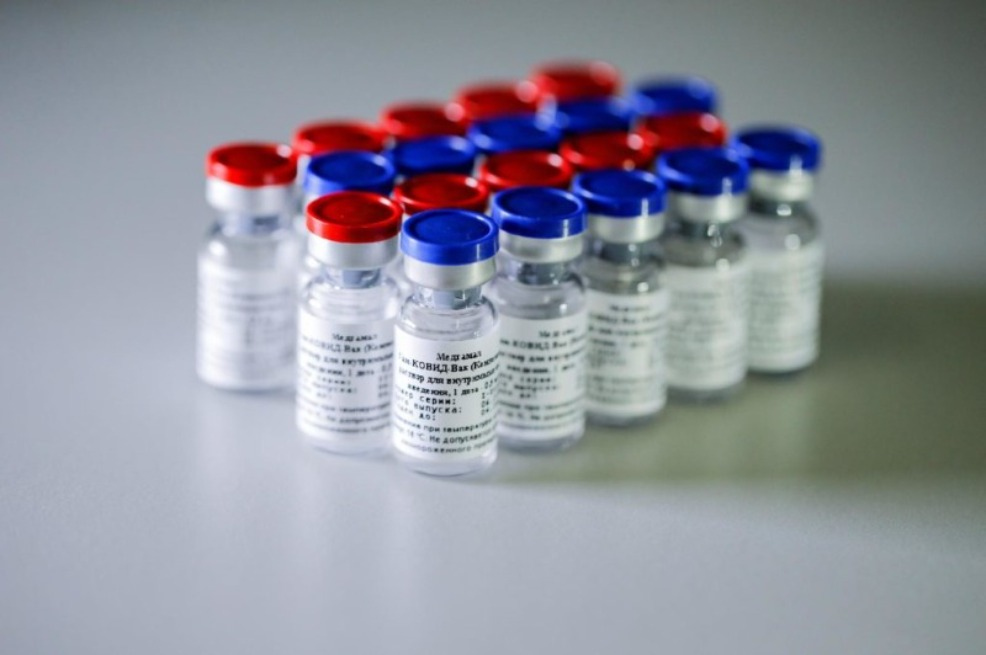
The Russian Direct Investment Fund (RDIF)/Handout via REUTERS)
A Anvisa (Agência Nacional de Vigilância Sanitária) negou nesta segunda-feira (26), durante reunião, o pedido de importação da Sputnik V, a vacina contra a Covid-19 desenvolvida na Rússia. O pedido já havia sido feito por 14 estados brasileiros, incluindo dois municípios do Rio de Janeiro.
A agência foi pressionada para decidir sobre os pedidos após determinação do ministro do STF (Supremo Tribunal Federal), Ricardo Lewandowski, em atendimento a ações de estados brasileiros, entre estes alguns já haviam comprado o imunizante e pretendiam aplicá-lo por conta própria.
A decisão dos cinco diretores da Anvisa teve críticas à falta de dados e a falhas graves de segurança da vacina.
O diretor-relator, Alex Machado, afirmou que em nenhuma das solicitações de importações foi apresentado o relatório técnico da vacina russa produzida por autoridades sanitárias internacionais que pudesse atestar que a Sputnik V atende a padrões de qualidade, eficácia e de segurança pré-estabelecidos. Além disso, Machado também diz que há falhas relacionadas ao controle da tecnologia usada para a fabricação da vacina, a de adenovírus vetor. Segundo ele, a detecção do vírus replicante – e não inativado, que não causa a doença – nas doses estudadas pela Anvisa poderia trazer séries riscos aos imunizados com a vacina.
“A presença de vírus replicante diverge do perfil de qualidade das vacinas com base em adenovírus avaliados pela Anvisa até o momento [...] e diverge também da apresentação da vacina Sputnik V, que garantiu a não replicação do vírus. Vírus não desejados estão na vacina e como o desenvolvimento não foi conduzido de forma a garantir a não replicação, a Sputnik V não cumpre o próprio critério estabelecido para seu desenvolvimento” , disse o relator.
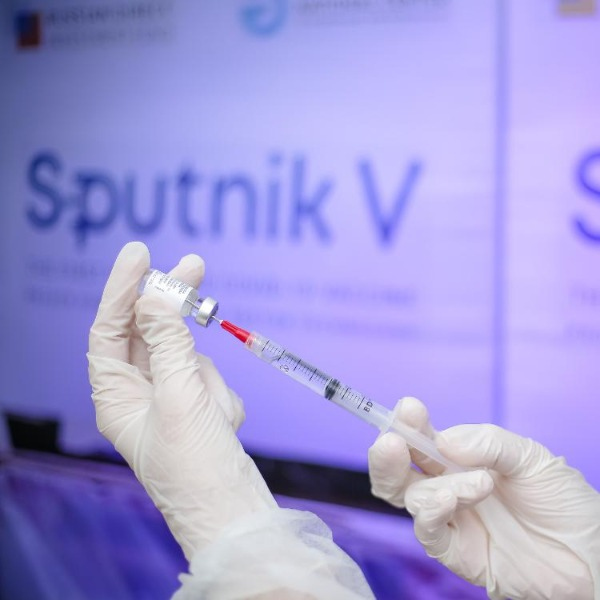
(Foto: Divulgação)
A diretora Meiruze Freitas, explicou os riscos caso os adenovírus se repliquem no corpo humano:
“Os adenovírus possuem uma gama de hospedeiros que podem causar infecções em humanos, algumas infecções leves no trato respiratório e gastrointestinal, mas as infecções induzidas por adenovírus podem ser fatais em pessoas imunocomprometidas, com distúrbio respiratório ou em cardiaco preexistente”.
Referente a autorização em outros países, Machado disse que, em sua maioria, os países não possuem participação em fóruns internacionais, nem contam com maturidade de avaliação pela OMS (Organização Mundial de Saúde). O relator ainda destaca que a Rússia vacinou apenas 8% da sua população, mesmo tendo um imunizante de fabricação própria.
“A vacina não está em uso em 23 países que a adquiriram [...] e em outros, contam com baixo contingente de pessoas que a receberam, o que ainda não permite conclusões sobre a segurança da vacina”.
Meiruze acrescenta as dificuldade pela agência para acessar as informações técnicas da vacina russa.
“Desde janeiro de 2021 estamos usando todos os canais para buscar as informações sobre qualidade, segurança e eficácia, e estamos até aqui sem os dados técnicos para que eu possa me dirigir à população e falar que os benefícios superam os riscos. Toda vez que um brasileiro ou brasileira recebe uma dose da vacina contra a covid-19, eles precisam ter a confiança dos servidores públicos da Anvisa”, destacou.
"Não foram apresentados dados de estudos clínicos e não clínicos. Nós, como diretores da Anvisa, fomos exaurientes na busca de informações e dados minimamente suficientes para garantir a proteção desta vacina”, acrescentou.
Entretanto, Meiruze reconheceu a credibilidade da Sputnik V, considerando a quantidade de países onde a vacina já é aplicada, e afirmou que poderia mudar a decisão caso mais dados sejam apresentados.
Já o diretor-presidente da Anvisa, Antonio Barra Torres, disse que a análise técnica da própria agência, exposta na mesma sessão, antes do voto dos diretores, que recomendou por não importar a vacina.
"Precisaríamos de argumentos muito fortes para votar contrariarmente. Caso a vacina cause revezes à saúde da população, não poderíamos nos escudar em uma ignorância quanto aos riscos do produto", comentou.
POR: Tamiris Felix
ÚLTIMAS
+LEIA TAMBÉM: Bolsonaro entra em contato com Putin sobre compra e produção da vacina "Sputnik V"
+LEIA TAMBÉM: França registra 5 novos casos de trombose após aplicação da vacina da "AstraZeneca/Oxford"
+LEIA TAMBÉM: Nova vacina chinesa tem autorização da Anvisa para ser testada no Brasil